VioletaStoimenova / Getty Images
Viktiga takeaways
- FDA har ett nära samarbete med tillverkarna om säkerhets- och effektivitetsdata som de förväntar sig för att överväga att godkänna ett COVID-19-vaccin.
- FDA planerar att sammankalla en extern rådgivande kommitté för att granska uppgifterna om varje COVID-19-vaccin som ansöker om tillstånd.
- Företag som får tillstånd för nödanvändning för ett COVID-19-vaccin måste fortsätta sina kliniska prövningar för att ge information på längre sikt om säkerhet och effektivitet.
- FDA förväntar sig att företag som beviljas tillstånd för nödsituationer också ska ansöka om ett standardgodkännande utan nödsituation.
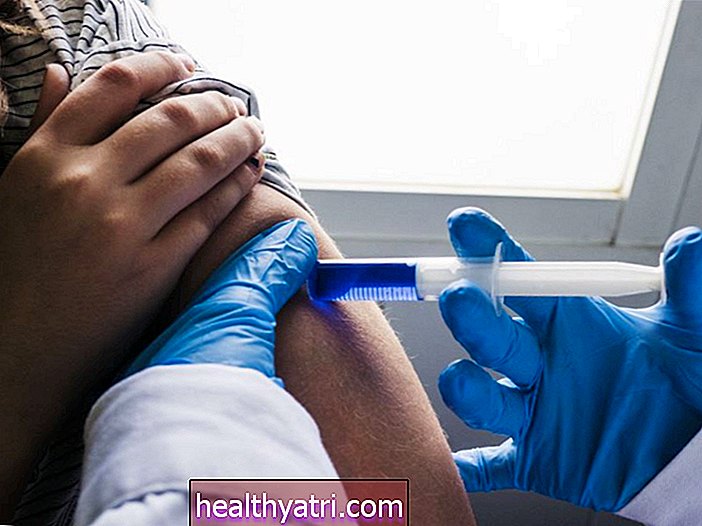
I dag sammankallade Food and Drug (FDA) för andra gången på en vecka sina rådgivande kommittéer för vacciner och relaterade biologiska produkter för att rekommendera ett ”nödanvändningsbehörighet” (EUA) för ett nytt COVID-19-vaccin från Moderna.
Det första COVID-19-vaccinet, tillverkat av Pfizer-BioNTech, godkändes av FDA förra veckan, och vaccinationer av vissa sjukvårdspersonal - de första personer som utsågs att få vaccinet - började i USA förra måndagen.
Men vad är en EUA exakt?
EUA-programmet inrättades 2004, i efterdyningarna av terrorattacken den 11 september 2001 i USA, för att godkänna användningen av en icke godkänd medicinsk produkt eller en icke godkänd användning av en godkänd medicinsk produkt under en deklarerad folkhälsoced. COVID-19 grundades som en nödsituation för folkhälsan i USA av minister för hälsa och mänskliga tjänster Alex Azar den 31 januari 2020.
COVID-19-vacciner: Håll dig uppdaterad om vilka vacciner som finns, vem som kan få dem och hur säkra de är.
"När det finns en förklarad nödsituation kan FDA göra en bedömning att det är värt att släppa något för användning även utan alla bevis som fullt ut skulle kunna fastställa dess effektivitet och säkerhet", säger Joshua Sharfstein, en tidigare chefsekreterare vid FDA, till Verywell . Sharfstein är nu vice dekan för folkhälsoutövning och samhällsengagemang vid Johns Hopkins Bloomberg School of Public Health i Baltimore, Maryland.
EUA utfärdades tidigare för läkemedel eller vacciner för att behandla eller förebygga mjältbrand, ebola och Mellanöstern respiratoriskt syndrom (MERS), säger Sharfstein.
EUA ansökningskrav
En tillverkare kan ansöka om en EUA - i motsats till ett mer formellt godkännande av en biologisk licensansökan (BLA) - om det inte finns något annat vaccin tillgängligt för att förhindra tillståndet. Dessutom måste FDA bestämma de kända och potentiella fördelarna med vaccinet uppväger riskerna med att få det.
"[För en EUA] finns det i allmänhet mindre data än vad som skulle ha varit tillgängligt för [en BLA]", säger LJ Tan, strategichef för Immunization Action Coalition, en advokatgrupp som arbetar för att öka immuniseringsgraden i USA, till Verywell. "Men det är inte att säga att de kliniska prövningarna äventyras i designen. Det är bara att EUA utfärdas tidigare än licensiering, så vi kommer inte att ha så mycket data som samlats in för försöket ännu."
Enligt FDA måste produkter som lämnas in för en EUA fortfarande testas noggrant. I oktober delade FDA branschens vägledning om vad de skulle leta efter när det gäller säkerhets- och effektivitetsdata för COVID-19-vacciner, inklusive data från studier om vaccinsäkerhet, plus minst två månaders uppföljning efter klinisk prövning. kompletteringar.
Enligt riktlinjerna kan FDA bevilja en EUA för ett vaccin om:
- Produkten kan med rimlighet förhindra, diagnostisera eller behandla sådan allvarlig eller livshotande sjukdom eller tillstånd som kan orsakas av SARS-CoV-2.
- De kända och potentiella fördelarna uppväger de kända och potentiella riskerna.
- Det finns inget adekvat, godkänt och tillgängligt alternativ till produkten för diagnos, förebyggande eller behandling av sjukdomen eller tillståndet.
FDA förväntar sig att vaccintillverkare ska inkludera en plan för uppföljning av vaccins säkerhet - som omfattar undersökning av rapporter om dödsfall, sjukhusvistelser och andra allvarliga eller kliniskt signifikanta biverkningar - bland individer som får vaccinet enligt en EUA.
"Att vara öppen och tydlig om de omständigheter under vilka utfärdande av ett tillstånd för nödanvändning för ett COVID-19-vaccin skulle vara lämpligt är avgörande för att bygga allmänhetens förtroende och säkerställa användningen av COVID-19-vacciner när de är tillgängliga", Peter Marks, MD, PhD, chef för FDA: s Center for Biologics Evaluation and Research, sa i ett uttalande. ”Förutom att beskriva våra förväntningar på vaccinsponsorer hoppas vi också att byråns vägledning om COVID-19-vacciner hjälper allmänheten att förstå vår vetenskapliga baserade beslutsprocess som säkerställer vaccinkvalitet, säkerhet och effekt för alla vacciner som är godkända eller godkända . "
FDA förväntar sig också att tillverkare som får en EUA fortsätter sina kliniska prövningar och slutligen ansöker om en BLA. En EUA är inte längre giltig när en folkhälsodeklaration inte längre är i kraft, vilket innebär att fullständigt godkännande krävs för att vaccinet ska kunna fortsätta att användas.
Vad detta betyder för dig
Food and Drug Administration tillåter företag att ansöka om tillstånd för COVID-19 enligt ett förfarande som kallas ett tillstånd för nödsituationer som kan påskynda den tid det tar att få ett vaccin godkänt.