
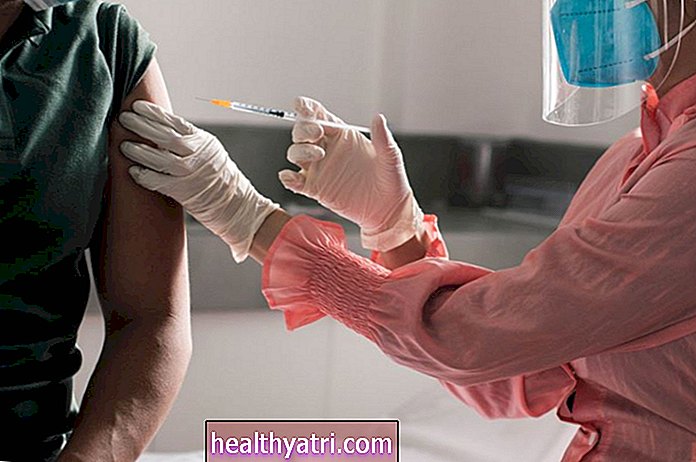
Sasiistock / Getty Images
Viktiga takeaways
- Pfizer har fått FDA-godkännande för att börja testa sitt coronavirusvaccin hos barn 12 år och äldre.
- Experter säger att inkludering av barn i kliniska prövningar är avgörande för den övergripande utvecklingen av ett vaccin som skyddar både barn och vuxna från COVID-19.
- Enligt sin webbplats har Pfizer redan registrerat mer än 39 000 volontärer i sin studie. Mer än 34 000 av dessa volontärer har redan fått en andra vaccination.
Pfizer, ett amerikanskt läkemedelsföretag, meddelade i oktober att det har fått tillstånd från U.S. Food and Drug Administration (FDA) att börja registrera barn så unga som 12 år i sina coronavirusvaccinförsök.
"Genom att göra detta kommer vi att kunna bättre förstå vaccinets potentiella säkerhet och effekt hos individer från fler åldrar och bakgrund", säger företaget i ett uppdaterat uttalande.
Detta kommer att vara den första COVID-19-vaccinförsöket i USA som inkluderar barn. Från och med oktober är Pfizer ett av fyra amerikanska företag som har vacciner i kliniska fas 3-studier.
Pfizer hade redan utvidgat fas 3 i sin försök till att omfatta barn 16 år och äldre, liksom personer med kroniskt, stabilt humant immunbristvirus (HIV), hepatit C och hepatit B.
Varför testa ett COVID-19-vaccin hos barn?
Innan Pfizer fick godkännande för att börja testa hos barn publicerade experter en rapport i tidskriftenKliniska infektionssjukdomarom vikten av sådan testning.
"Den direkta effekten av COVID-19 på barn är större än vad som observerats för ett antal andra patogener som vi nu har effektiva pediatriska vacciner för", konstaterar rapporten. ”Dessutom har barnens roll i SARS-CoV-2-överföringen uppenbarligen inte uppskattats. Noggrant utförda kliniska fas 2-studier kan på ett adekvat sätt ta itu med potentiella COVID-19-vaccinsäkerhetsproblem. ”
Suzanne Pham, MD
Vi kan inte övervinna spridningen av detta virus om vi inte vaccinerar våra barn.
- Suzanne Pham, MDSharon Nachman, MD, chef för avdelningen för pediatriska infektionssjukdomar vid Stony Brook Children's Hospital i New York, instämmer i rapporten och säger till Verywell att ”barnläkare är mycket intresserade av att se detaljerna i studien och hur kommer vaccinet att fungera hos barn . ”
Det finns specifika fördelar med att testa vaccinet hos barn, enligt Nachman. Forskarna kommer att kunna bedöma immunsvaret på kort och lång sikt, vilket inkluderar att ta reda på om vaccindosen som används hos vuxna är nödvändig för barn, eller om de skulle ha ett liknande immunsvar till en lägre dos.
Nachman säger att det också är viktigt att notera att eftersom koronavirus hos vuxna kan föregås av deras exponering för en asymptomatisk infektion hos barn, kan etablering av ett vaccin för att behandla en hel familj "gå långt för att minska överföringen hemma och i samhället."
Suzanne Pham, MD, biträdande medicinsk chef på Weiss Memorial Hospital i Chicago, berättar för Verywell att ju tidigare barn kan vaccineras, desto snabbare kommer överföringshastigheterna att minska.
"Genom att effektivt vaccinera barn minskar risken för att barn överför viruset i samhället, särskilt för de högriskpersoner som är mer mottagliga för svår eller kritisk sjukdom", säger Pham till Verywell. ”Detta gör det möjligt för skolor att börja återuppta och aktiviteter som är viktiga för att våra barns utveckling ska återupptas på ett kontrollerat sätt. Vi kan inte övervinna spridningen av detta virus om vi inte vaccinerar våra barn. Vi måste ha tillräckligt med flockimmunitet i samhället för att kunna förhindra spridning. ”
COVID-19-vacciner: Håll dig uppdaterad om vilka vacciner som finns, vem som kan få dem och hur säkra de är.
Hur börjar vaccinförsök?
Pham förklarar att för att ett vaccin ska kunna testas - på vuxna eller barn - måste ett företag först lämna in en utredningsansökan (FDA).
Applikationen beskriver vaccinet, hur det tillverkas och vilka kvalitetskontrollstest som ska användas. Ansökan innehåller också data från djurförsök som visar att vaccinet är säkert för inledande testning på människor.
Som FDA förklarar har ansökningsprocessen flera steg:
Under ett nytt läkemedels tidiga prekliniska utveckling är sponsorens primära mål att avgöra om produkten är rimligt säker för initial användning hos människor och om föreningen uppvisar farmakologisk aktivitet som motiverar kommersiell utveckling.
När en produkt identifieras som en livskraftig kandidat för vidareutveckling fokuserar sponsorn sedan på att samla in den information och information som är nödvändig för att fastställa att produkten inte kommer att utsätta människor för orimliga risker när de används i begränsade kliniska studier i ett tidigt stadium.
Vaccinet kommer sedan att genomgå fas 1-prövningar, vilket Pham förklarar är "säkerhets- och immunogenicitetsstudier utförda på ett litet antal människor som övervakas noggrant."
"Fas 2 består av dosomfattande studier och utvidgas till större antal (hundratals) människor", säger Pham. "Sedan försöker fas 3-studier att registrera tusentals människor för att dokumentera effektiviteten och fortsätta titta på säkerhetsdata."
Enligt sin webbplats har Pfizer registrerat mer än 39 000 volontärer i sin studie. Mer än 34 000 av dem har fått en andra dos av vaccinet.
Vad detta betyder för dig
En klinisk fas 3-studie som inkluderar testning av ett COVID-19-vaccin hos barn är ett tecken på framsteg. Ett vaccin kan dock inte skyndas. Att slutföra resultaten tar tid att skydda försöksdeltagarnas säkerhet, såväl som vuxna och barn som så småningom får den färdiga versionen av vaccinet.


















-is-common-in-autism.jpg)