wera Rodsawang / Getty Images
Viktiga takeaways
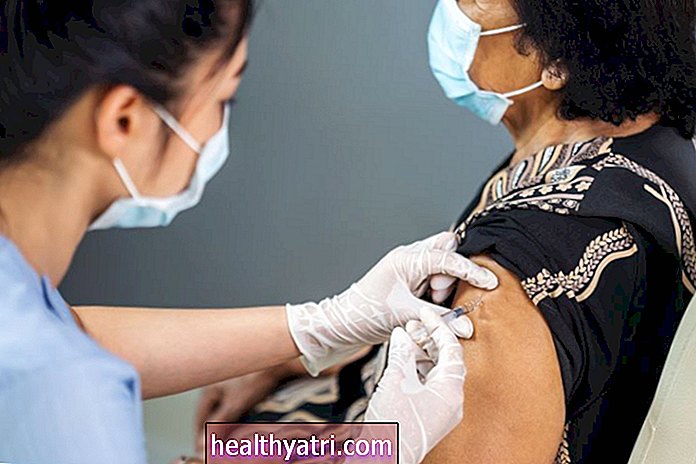
- Ett nytt budbärar-RNA-vaccin (mRNA) blev det första COVID-19-vaccinet som godkänts för akut användning i USA.
- Forskare arbetar med tio olika befintliga vaccinmodeller för att skapa COVID-19-vacciner
- Ett vaccin måste vara minst 70% effektivt för att utrota COVID-19
- Att snabbt spåra ett vaccin innebär att kringgå skyddsåtgärder
Tävlingen för att hitta ett säkert och effektivt vaccin mot COVID-19 (coronavirus sjukdom 2019) är utan föregång i modern medicinsk historia. Inte sedan aids-pandemin om 1980- och 90-talet har forskare, regeringar och företag tillsammans i ett samordnat försök att dela kunskap och resurser som en dag kan leda till utvecklingen av ett helt skyddande vaccin.
Som med aids-pandemin är det mycket som forskare måste lära sig om viruset.
Men det finns hopp. Från och med december 2020 fanns inte mindre än 233 vaccinkandidater i aktiv utveckling i Nordamerika, Europa och Asien, med målet att minst ett helt ut på marknaden 2021.
Den 11 december beviljade Food and Drug Administration (FDA) tillstånd för akut användning för en COVID-19-vaccinkandidat som utvecklats av Pfizer och BioNTech. Denna akutanvändning är godkänd för personer i åldrarna 16 år och äldre. En annan COVID-19-vaccinkandidat från Moderna beviljades tillstånd för akut användning den 18 december. Båda vaccinerna är nya budbärar-RNA (mRNA) -vacciner som innehåller genetiska instruktioner för våra immunceller för att göra en del av ett protein som utlöser ett immunsvar mot COVID -19.
Varför det här är viktigt?
Så skrämmande som utmaningarna kan tyckas är ett vaccin fortfarande det mest effektiva sättet att förhindra de globala blockeringar och sociala distansåtgärder som definierade den tidiga COVID-19-pandemin.
Mål och utmaningar
Själva tidslinjen innebär enorma utmaningar. Med tanke på att vacciner tar i genomsnitt 10,71 år att utvecklas från början av preklinisk forskning till de slutgiltiga myndighetsgodkännandena, har forskarna i uppgift att komprimera tidslinjen på ett sätt som i stort sett är okänt i vaccinforskningen.
För att ett vaccin ska kunna betraktas som livskraftigt måste det vara säkert, billigt, stabilt, enkelt tillverkat i produktionsskala och enkelt administreras till så många av de 7,8 miljarder människor som bor på planeten som möjligt.
Samtidigt, om ett vaccin ska avsluta pandemin, måste det ha en hög effektivitetsnivå, ännu högre än influensavaccinets. Allt annat än detta kan mildra spridningen av infektioner, men inte stoppa dem.
Endast 6% av vaccinerna under utveckling gör från preklinisk forskning till marknadsutsläpp.
Vaccineffektivitet
Enligt Världshälsoorganisationen (WHO), för att ett vaccin ska kunna utrota COVID-19, måste det vara minst 70% effektivt på befolkningsbasis och ge ett bestående skydd i minst ett år. På denna nivå skulle viruset kunna muteras mindre eftersom det passerar från person till person och mer sannolikt att generera flockimmunitet (där stora delar av befolkningen utvecklar immunresistens mot viruset).
Dessa riktmärken är otroligt ambitiösa, men inte omöjliga.
Vid 60% effektivitet hävdar WHO att utbrott fortfarande skulle inträffa och att flockimmuniteten inte skulle byggas tillräckligt aggressivt för att stoppa pandemin.
Ett COVID-19-vaccin med 50% effektivitet, även om det är till nytta för högriskindivider, skulle varken förhindra utbrott eller minska stressen i frontlinjens hälsovårdssystem om ett utbrott inträffar.
Effekten av influensavaccinet var till exempel mindre än 45% under influensasäsongen 2019--2020, enligt Centers for Disease Control and Prevention (CDC). Vissa av de enskilda vaccinkomponenterna var endast 37% effektiva.
mRNA-vacciner för COVID-19
Pfizer tillkännagav den 18 november att dess vaccin fas III-studie visade 95% effektivitet mot COVID-19. Moderna meddelade den 30 november att dess vaccin fas III-studie visade 94% effektivitet mot COVID-19 totalt och också 100% effektivitet mot svår sjukdom Peer review granskas fortfarande för dessa försök.
Hälsovårdsmyndigheter kan godkänna ett vaccin med mindre än optimal effekt om fördelarna (särskilt för äldre och fattiga) överväger riskerna.
Kosta
Ett vaccin kan inte betraktas som livskraftigt om det inte är överkomligt.
Till skillnad från influensavaccinet, som massproduceras genom att injicera viruset med kycklingägg, kan varken COVID-19 eller någon av dess koronavirus-kusiner (som SARS och MERS) reproduceras i ägg. Därför behövs en helt ny produktionsteknik för att matcha produktionsvolymen för det årliga influensavaccinet, varav över 190 miljoner doser levereras i USA varje år.
Nya genetiska vacciner, inklusive Pfizer-BioNTech- och Moderna-vaccinkandidaterna, utvecklas i provrör eller tankar. De behöver inte odlas i ägg eller celler, vilket sparar tid och kostnader i utvecklingen. Även om detta är första gången de skulle massproduceras så fulla kostnader och många logistik är fortfarande okända.
USA har avtal om att köpa doser av mRNA-vaccinkandidaterna från Pfizer-BioNTech och Moderna, men kostnaderna och tillgängligheten för dessa vacciner och andra i många länder över hela världen är fortfarande obestämda.
Den amerikanska regeringen har ett kontrakt med Pfizer och BioNTech för en initial order på 100 miljoner doser för 1,95 miljarder dollar och rättigheterna att förvärva upp till 500 miljoner ytterligare doser. De som får vaccinet får det gratis. Vaccinet har också fått tillstånd för akut användning i Storbritannien, Bahrain, Saudiarabien, Kanada och Mexiko.
Den federala regeringen har ett kontrakt på 1,5 miljarder dollar med Moderna om 100 miljoner doser av vaccinet och möjligheten att förvärva ytterligare 400 miljoner doser (den har redan begärt ytterligare 100 miljoner doser). Det hjälpte också till att finansiera utvecklingen med ett kontrakt på 955 miljoner dollar, vilket innebar att den initiala summan uppgick till 2,48 miljarder dollar. Om den får nödtillstånd kommer den också att ges gratis till människor i USA.
Distribution
Efter att COVID-19-vacciner har utvecklats är nästa utmaning att fördela dem rättvist, särskilt om produktionskapaciteten är begränsad. Detta kräver omfattande epidemiologisk forskning för att avgöra vilka populationer som har störst risk för sjukdom och död.
För att undvika dessa farhågor rekommenderade vissa experter att finansieringen riktas till beprövade vaccinmodeller som är mer benägna att vara skalbara snarare än experimentella som kan kräva miljarder dollar i strukturella investeringar innan den första tilldelningen av vaccinet är ens. produceras.
Stora investeringar gjordes på experimentella, men även om de utgör utmaningar för massdistribution, inklusive potentiella kostnader och ultrakalla temperaturkrav för Pfizer-BioNTech-vaccinet som behöver specialiserade frysar.
Pfizer och BioNTech projicerar en global produktion på upp till 50 miljoner doser 2020 och upp till 1,3 miljarder doser i slutet av 2021. Moderna projicerar en produktion på cirka 20 miljoner doser redo att skickas i USA vid slutet av 2020 och en global produktion på 500 miljoner till 1 miljard doser 2021.
Etiska dilemman
Snabbspårning av ett vaccin minimerar vissa kontroller och balanser som är utformade för att skydda människor. Detta betyder inte att det är omöjligt att göra det. Det kräver helt enkelt större övervakning från tillsynsmyndigheter som WHO, National Institutes of Health (NIH), Europeiska läkemedelsmyndigheten (EMA) och kinesiska Food and Drug Administration (CFDA) för att säkerställa att forskning bedrivs säkert och etiskt.
Även med större tillsyn över lagstiftningen har loppet att producera ett marknadsfärdigt vaccin inom två år väckt oro bland etikister som hävdar att du inte kan utveckla ett vaccin snabbtochsäkert.
"Utmaningsstudier" involverar till exempel rekrytering av tidigare oinfekterade, friska, unga vuxna som direkt exponeras för COVID-19 efter att ha genomgått vaccination med kandidatvaccinet. Om ett utmaningsvaccin visar sig vara säkert och effektivt i denna låg risk gruppen skulle nästa steg vara att rekrytera vuxna med högre risk i en traditionell dubbelblind prövning. Medan utmaningar som detta används med mindre dödliga sjukdomar, som influensa, är det avsevärt riskabelt att utsätta människor för COVID-19.
När COVID-19-forskning går från prekliniska studier till större mänskliga prövningar kommer dilemman som denna att sätta press på tillsynsmyndigheterna för att avgöra vilka risker i denna nya gräns som är "acceptabla" och vilka som inte är.
Var ska man börja?
Forskare börjar inte från början när de utvecklar sina COVID-19-vaccinmodeller (kallade plattformar). Det finns inte bara effektiva vacciner baserade på relaterade virus utan experimentella som har visat partiellt skydd mot koronavirus som MERS och SARS.
COVID-19 tillhör en stor grupp av virus som kallas RNA-virus som inkluderar ebola, hepatit C, HIV, influensa, mässling, rabies och en mängd andra infektionssjukdomar. Dessa är vidare uppdelade i:
- Grupp IV-RNA-virus: Dessa inkluderar koronavirus, hepatitvirus, flavivirus (associerad med gul feber och West Nile feber), poliovirus och rhinovirus (ett av flera förkylningsvirus
- Coronaviridae: En familj av grupp IV-RNA-virus som inkluderar fyra koronavirusstammar kopplade till förkylning och tre som orsakar allvarlig andningssjukdom (MERS, SARS och COVID-19)
Insikt från dessa virus, hur liten som helst, kan ge forskare de bevis som behövs för att bygga och testa sina plattformar. Även om en plattform misslyckas kan den peka forskare i riktning mot mer livskraftiga.
Till och med bland de många grupp IV-RNA-virusen har endast en handfull vacciner (polio, röda hund, hepatit A, hepatit B) utvecklats sedan det första gula febervaccinet 1937. Hittills finns inga vacciner mot koronavirus som är helt godkända och licensierade i USA.
Modeller för vaccinutveckling
Loppet för att hitta ett effektivt COVID-19-vaccin koordineras till stor del av WHO och globala partner som den nyligen bildade Coalition for Epidemic Preparedness Innovations (CEPI). Dessa organisationers roll är att övervaka forskningslandskapet så att resurser kan riktas till de mest lovande kandidaterna.
CEPI skisserade de olika plattformarna som COVID-19 kunde bygga på. Vissa är uppdaterade modeller baserade på Salk- och Sabin-poliovaccinerna på 1950- och 60-talet. Andra är nästa generations vacciner som är beroende av genteknik eller nya leveranssystem (kallade vektorer) för att rikta in sig på andningsceller.
proteinvacciner
Det finns fördelar och nackdelar med var och en av de föreslagna plattformarna. Vissa av vaccintyperna tillverkas lätt i produktionsskala men är mer generaliserade i sitt svar (och är därför mindre benägna att nå de effektivitetsnivåer som behövs för att avsluta pandemin). Andra nyare modeller kan framkalla ett starkare svar, men lite är känt om vad vaccinet kan kosta eller om det kan produceras i global skala.
Av de tio vaccinplattformar som CEPI skisserat har fem aldrig producerat ett livskraftigt vaccin hos människor. Ändå har vissa (som DNA-vaccinplattformen) skapat effektiva vacciner för djur.
Vaccinutvecklingsprocess
Även om stadierna av vaccinutvecklingen komprimeras, kommer processen med att godkänna COVID-19-vacciner att förbli ungefär densamma. Stegen kan delas upp enligt följande:
- Prekliniskt stadium
- Klinisk utveckling
- Lagstadgad granskning och godkännande
- Tillverkning
- Kvalitetskontroll
Det prekliniska steget är den period under vilken forskare sammanställer genomförbarhets- och säkerhetsdata, tillsammans med bevis från tidigare studier, för att överlämna till statliga tillsynsmyndigheter för testgodkännande. I USA övervakar FDA denna process. Andra länder eller regioner har egna regleringsorgan.
Klinisk utveckling är det stadium där faktisk forskning utförs på människor. Det finns fyra faser:
- Fas I syftar till att hitta den bästa dosen med minst biverkningar. Vaccinet kommer att testas i en liten grupp med färre än 100 deltagare. Cirka 70% av vaccinerna klarar det här inledande steget.
- Fas II utvidgar testningen till flera hundra deltagare baserat på den dos som anses vara säker. Fördelningen av deltagare kommer att matcha den allmänna demografin för personer som riskerar COVID-19. Ungefär en tredjedel en fas II-kandidater kommer till fas III.
- Fas III involverar tusentals deltagare på flera platser som slumpmässigt väljs ut för att antingen få det verkliga vaccinet eller placebo. Dessa studier är vanligtvis dubbelblindade så att varken forskare eller deltagare vet vilket vaccin som administreras. Detta är det stadium där de flesta vacciner misslyckas.
- Fas IV äger rum efter det att vaccinet har godkänts och fortsätter i flera år för att utvärdera vaccinets verkliga effekt och säkerhet. Denna fas kallas också "övervakning efter marknadsföring".
COVID-19-vacciner: Håll dig uppdaterad om vilka vacciner som finns, vem som kan få dem och hur säkra de är.
Tidpunkt
Så enkelt som processen är, det finns flera saker bortom vaccinsvikt som kan lägga månader eller år till processen. Bland dem är timing. Även om en vaccinkandidat helst bör testas under ett aktivt utbrott, kan det vara svårt att veta var eller när en kan inträffa.
Även i hårt drabbade områden som New York City och Wuhan, Kina, där ytterligare utbrott verkar överhängande, kan folkhälsovården ingripa för att förebygga sjukdomar med åtgärder som att kräva att människor isoleras igen. Detta är viktigt för att hålla människor friska, men kan förlänga vaccinförsök över en hel säsong eller ett helt år.
Vaccinkandidater i rörledningen
Från och med december 2020 godkänns 56 vaccinkandidater för klinisk forskning, medan över 165 befinner sig i prekliniska steg och väntar på godkännande av myndighet.
Av de plattformar som är godkända för testning är inaktiverade vacciner bland de vanligaste. Detta inkluderar proteinunderenheter, som använder antigener (komponenter som bäst stimulerar immunsystemet) istället för hela viruset, och helcellsinaktiverade vacciner, varav några använder "boosting" -medel som aluminium för att öka antikroppssvaret.
RNA- och DNA-vacciner är också väl representerade, liksom vektoriserade vacciner som använder deaktiverade förkylningsvirus för att bära vaccinmedel direkt till celler.
Ytterligare plattformar inkluderar virusliknande partiklar, vektoriserade vacciner i kombination med antigenpresenterande celler och ett levande försvagat vaccin som använder en försvagad, levande form av COVID-19 för att stimulera ett immunsvar.
(Storbritannien)
(Kina)
(Förenta staterna)
(Förenta staterna)
(Förenta staterna)
(Kina)
(Kina)
(Kina)
(Förenta staterna)
(Kina)
(Förenta staterna)